突破体内药物递送瓶颈!中国科大揭示肝脏清除递送系统的底层机制
3月20日,中国科学技术大学王育才/朱书/蒋为团队在《科学》(Science)发表题为“Commensal-driven serotonin production modulates in vivo delivery of synthetic and viral vectors”的研究论文,报道了一项递送科学领域的突破性成果。团队阐明了一条由肠道共生菌与肠道内分泌系统共同维持的肠—肝免疫调控轴。该轴可持续驱动机体清除药物递送载体,严重制约递送技术应用。干预该轴可显著抑制机体对递送载体的非特异性清除、改善药物循环,使肿瘤递送效率提升2-3倍、靶组织基因编辑效率提升10-15倍,从而为肿瘤靶向治疗、mRNA疗法、基因编辑等技术提供普适性疗效增强策略。该发现从机制层面破解了困扰递送领域数十年的“载体非特异性清除”难题,为推动递送技术的临床转化提供了普适性方案。
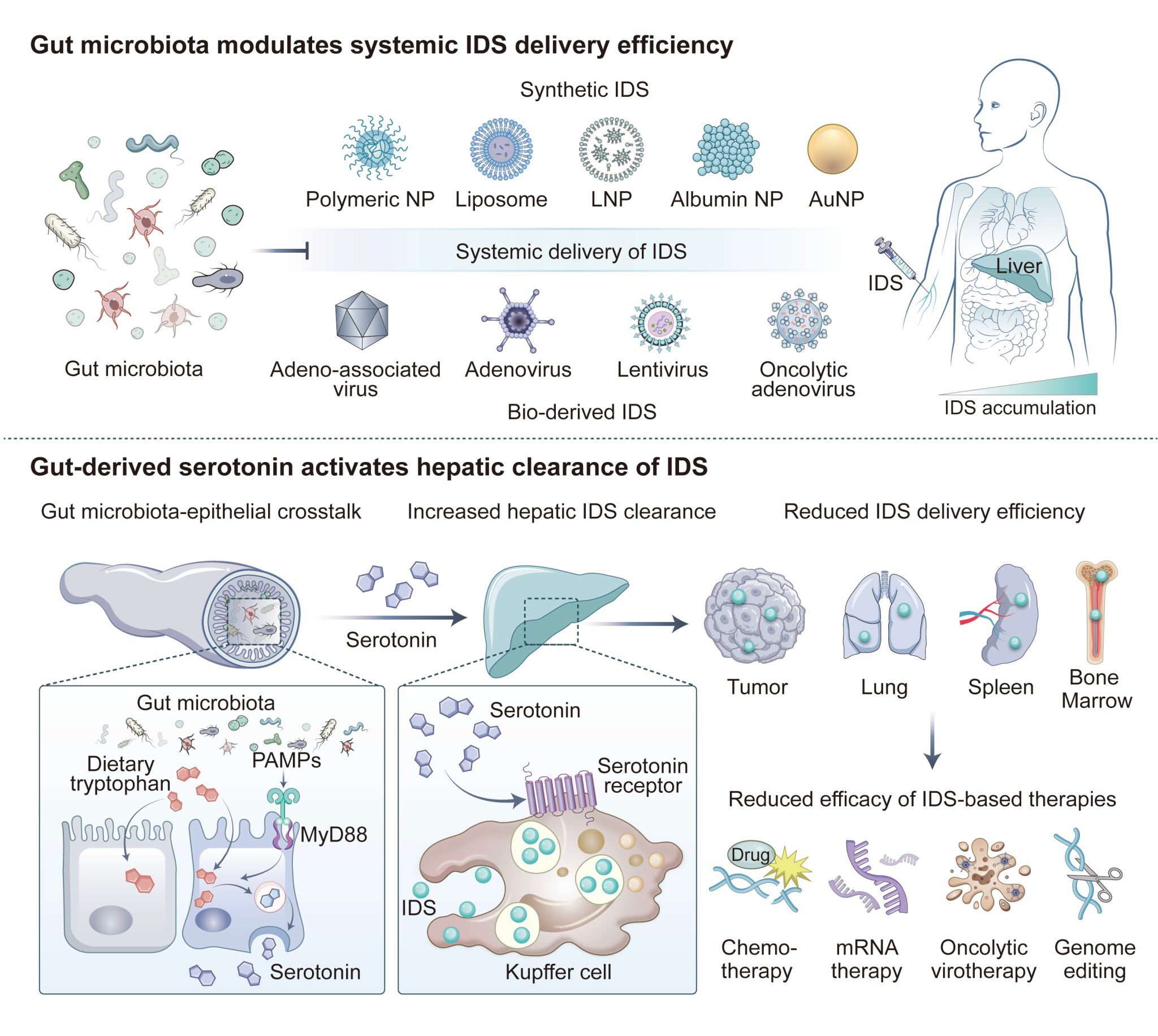
肠道共生菌通过刺激肠道五羟色胺分泌维持肝脏对递送载体的清除活性
临床药物应用常面临多重药理学挑战,包括系统毒性高、组织靶向性差(如化疗药物)、稳定性差(如核酸类药物)、生物利用度低(如脂溶性药物)等。递送载体通过对药物的高效封装、稳定保护与靶向递送,可有效解决上述难题,支撑相关药物转化,因而在现代生物医药领域占有重要地位。近十年来,递送技术已成功推动肿瘤靶向化疗、mRNA疫苗、基因疗法等治疗理念实现临床应用。然而,递送载体给药后普遍存在快速清除问题,导致到达靶标组织的药量极低(比如现有纳米药物向肿瘤的有效递送剂量可仅占总剂量的0.7%以下),严重制约治疗疗效。虽然已知单核吞噬系统是介导这一清除过程的主要细胞群体,但当前学术界仍缺乏安全普适的干预手段。递送领域对该问题长期陷入“现象描述—机制缺失—单纯载体筛选—效果有限且普适性差”的循环,难以突破这一核心瓶颈对递送领域发展的制约。
在本研究中,研究人员发现:清除小鼠的肠道共生菌可显著提升各类递送载体向肿瘤的递送效率,其中包括聚合物纳米颗粒、脂质纳米颗粒(LNP)、脂质体、白蛋白纳米颗粒以及溶瘤腺病毒。递送效率的提升可以直接转化为肿瘤化疗、溶瘤病毒疗法、蛋白替代疗法等抗肿瘤手段的疗效提升。肠道菌清除还能显著提升多器官基因递送效率,增加体细胞编辑效率。药代动力学研究发现,肠道菌清除可显著提升各类递送载体的血液循环能力,这解释了药物终端递送效率增加的现象。
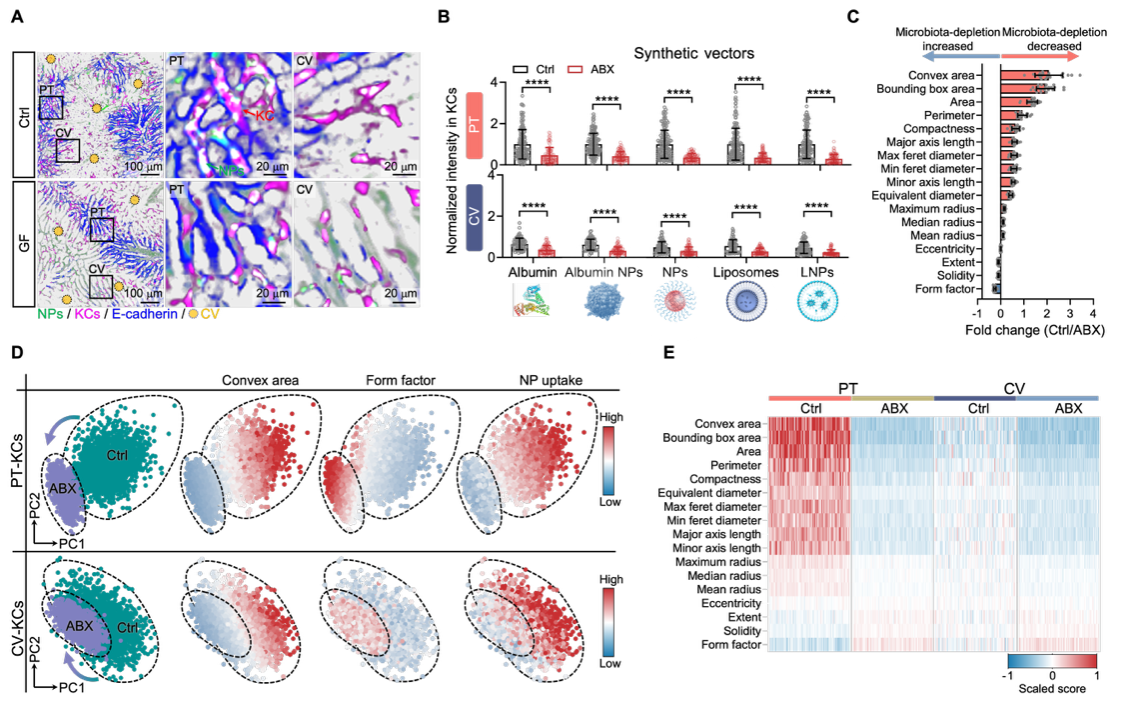
活体成像平台证明Kupffer细胞是肠道共生菌驱动载体清除的关键效应细胞
为研究肠道菌降低递送载体循环能力的机制。团队开发了一套基于活体成像的单细胞形态及载体互作行为定量分析系统,并绘制了单核巨噬系统在不同处理状态下的行为、形态学全景图谱。通过对多器官、多模型、多载体的系列研究,研究人员证实肝脏Kupffer细胞(KCs)是肠道菌影响药物递送的终端靶细胞群体。肠道菌清除可显著抑制KCs对各类递送载体的摄取能力,下降幅度可高达70%。这使得肝脏整体对各类递送载体的清除效率显著下降。
然而一系列机制实验暗示,肠道菌对KCs功能的调控可能需要宿主其他细胞群体进行信号转导实现。使用Cre-LoxP系统特异性敲除肝脏主要细胞群体对细菌的感受通路,都无法重现肠道菌清除带来的KCs行为改变。在对其他主要细胞群体进行基因敲除筛选后,团队发现肠道上皮细胞才是感受细菌,并调控肝脏免疫功能的核心信号枢纽。
进一步的,肠道上皮细胞如何实现对肝脏免疫系统的远距离调控?团队筛选了肠道上皮细胞代谢分子库,证实肠道内分泌系统来源的血清素正是沟通肠道菌和肝脏免疫系统的核心信使分子,至此,一条完整的递送调控轴被发现:肠道共生菌持续激活肠道上皮内分泌系统,促进生理状态下血清素的分泌;后者肝后激活KCs,提升其对各类递送载体的吞噬能力,导致载体循环能力受损,递送效率下降,最终在临床治疗过程中导致相关药物的疗效远低于预期。干预该血清素通路,或直接通过饮食调控限制色氨酸摄入,均可快速抑制KCs对递送载体的清除活性,显著提升载体的体内循环时间与靶组织递送效率,并在多种治疗模型中实现与肠道菌群清除同等显著的纳米药物疗效提升。
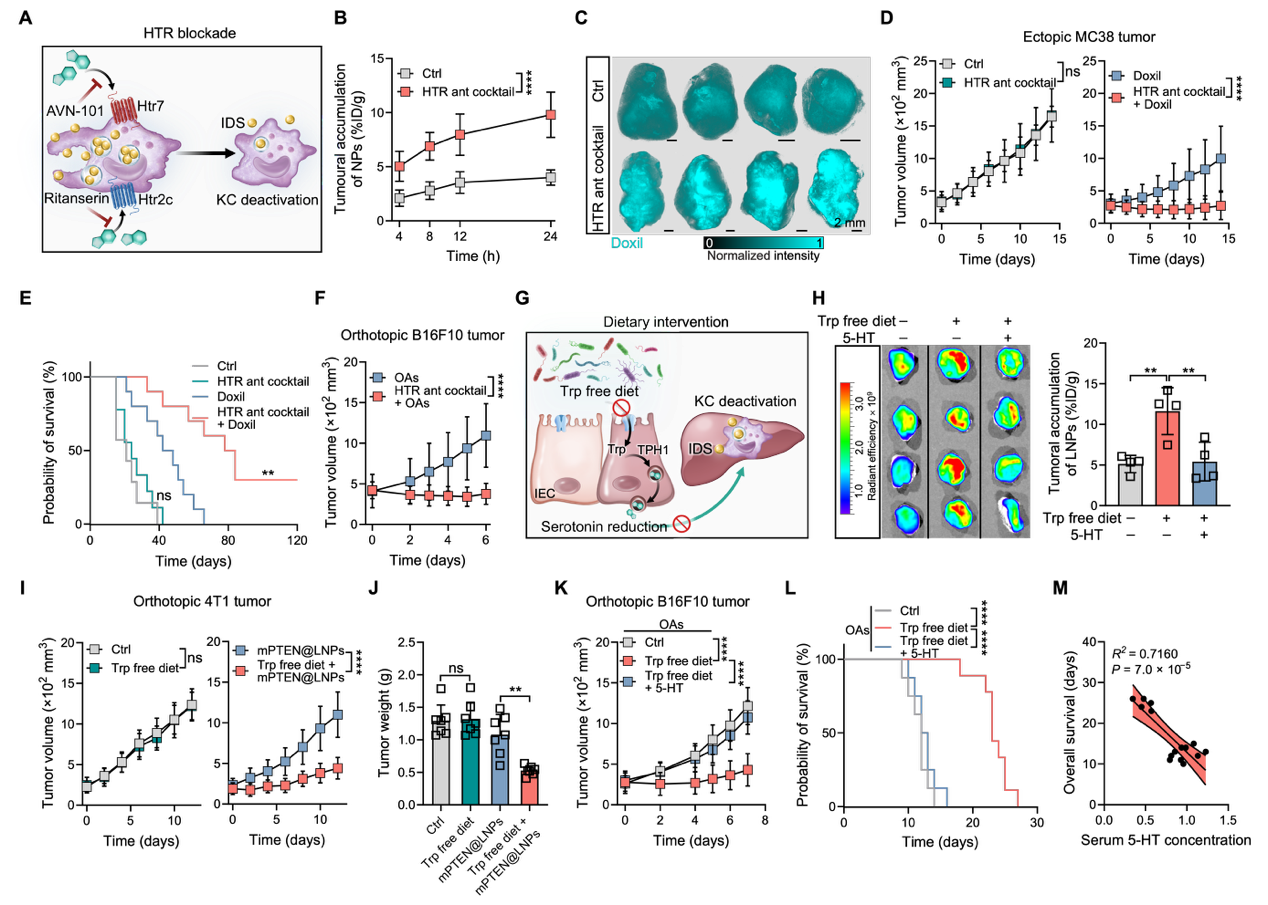
干预该调控轴可广谱性提升各类载体的递送效率
本研究揭示了驱动递送载体发生非选择性肝脏富集的底层机制,为药物递送载体的设计与应用提供了理论框架;从转化应用角度看,本研究提供了一系列可快速向临床转化的递送辅助策略,并利用多种临床获批药物在多种疾病模型中完成临床前疗效验证,为推动药物递送相关疗法的发展、工程化制备与临床转化提供了新视角与新方法。
中国科大王育才教授、朱书教授、蒋为教授为本论文的共同通讯作者,中国科大汪沁博士、博士生陈子琦、张国荣特任副研究员为该论文共同第一作者。中国科学技术大学附属第一医院张树庚主任为本研究提供了重要支持。本研究获国家自然科学基金、国家重点研发计划、中国科协青年人才托举工程、中国科学院战略性先导科技专项、安徽省自然科学基金等科技项目资助。

团队主要成员合影
论文链接:https://www.science.org/doi/10.1126/science.adu7686
(生命科学与医学部、科研部)