记者20日从中国科学技术大学获悉,该校王育才、朱书、蒋为教授团队首次阐明肠道共生菌与肠道内分泌系统共同维持的肠—肝免疫调控轴,揭示了机体非特异性清除药物递送载体的底层机制。相关研究成果3月20日发表于《科学》。
药物递送载体能有效解决化疗药物系统毒性高、核酸药物稳定性差、脂溶性药物生物利用度低等问题,长期以来,递送载体给药后易被机体快速清除,导致靶标组织药量极低,严重制约治疗疗效,且学界缺乏安全普适的干预手段。
研究团队开展系统性研究发现,清除小鼠肠道共生菌后,聚合物纳米颗粒、脂质纳米颗粒、溶瘤腺病毒等各类递送载体的肿瘤递送效率显著提升。递送效率的提升可以直接转化为肿瘤化疗、溶瘤病毒疗法、蛋白替代疗法等抗肿瘤手段的疗效提升。多器官基因递送与体细胞编辑效率也大幅增加,核心原因是载体的血液循环能力得到显著改善。
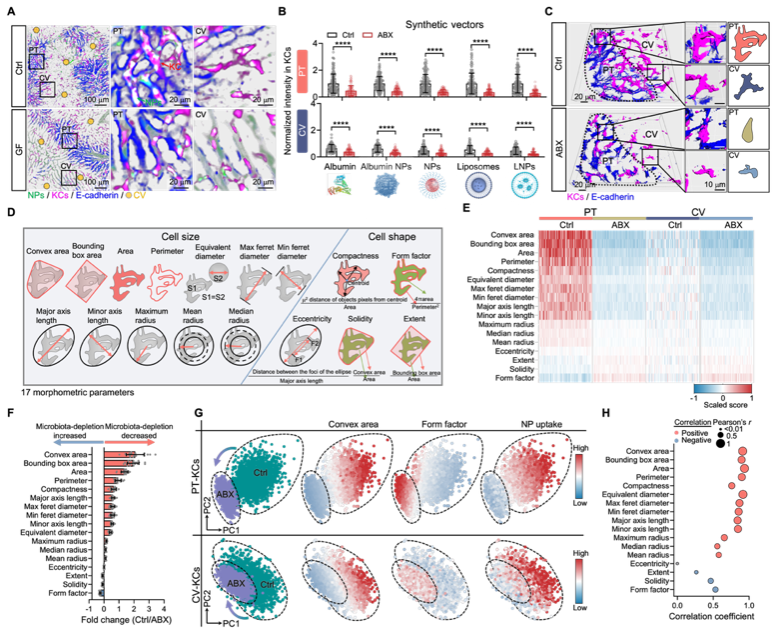
为解析机制,团队开发了基于活体成像的单细胞形态及载体互作行为定量分析系统,证实肝脏Kupffer细胞是肠道菌调控药物递送的终端靶细胞,肠道菌清除可使其对递送载体的摄取能力显著下降,下降幅度最高可达70%。进一步研究明确,肠道上皮细胞是感受细菌信号并调控肝脏免疫的核心枢纽,肠道内分泌系统分泌的血清素是沟通肠道菌与肝脏免疫系统的关键信使分子。
研究表明,肠道共生菌激活肠道上皮内分泌系统促进血清素分泌,血清素进而激活肝脏Kupffer细胞,增强其对递送载体的吞噬能力,导致载体循环受损、递送效率下降。实验也证实,干预该血清素通路或通过饮食调控限制色氨酸摄入,均可显著抑制肝脏Kupffer细胞对递送载体的清除活性,使肿瘤递送效率提升2—3倍、靶组织基因编辑效率提升10—15倍,在多种疗法等模型中均实现显著疗效提升。
研究人员表示,这项研究为破解困扰递送领域数十年的核心难题提供了普适性解决方案,显著提升肿瘤靶向治疗、mRNA疗法、基因编辑等疗法的递送效率与治疗效果,也为生物医药递送技术的临床转化开辟新路径。
记者:吴长锋 来源:科技日报 2026-03-20
原文链接:https://www.stdaily.com/web/gdxw/2026-03/20/content_489117.html