近日,中国科学技术大学闵元增教授团队在放射治疗增敏剂领域取得重大突破,有效解决了传统放射增敏剂毒副作用大、肿瘤特异性差、依赖活性氧等关键技术瓶颈。为精准放疗增敏与肿瘤免疫治疗的协同发展提供了全新思路和技术支撑。 放射治疗是肿瘤治疗的核心手段之一,通过直接或间接损伤肿瘤细胞DNA发挥杀伤作用,而放射增敏剂可增强肿瘤细胞对放射线的敏感性,同时减少对正常组织的损伤,实现低剂量、安全且高效得放疗。然而,目前的放射增敏剂多存在脱靶效应明显、无放疗时仍有毒副作用、缺乏肿瘤特异性等缺陷,且多数依赖活性氧生成实现增敏,其临床转化面临巨大挑战。
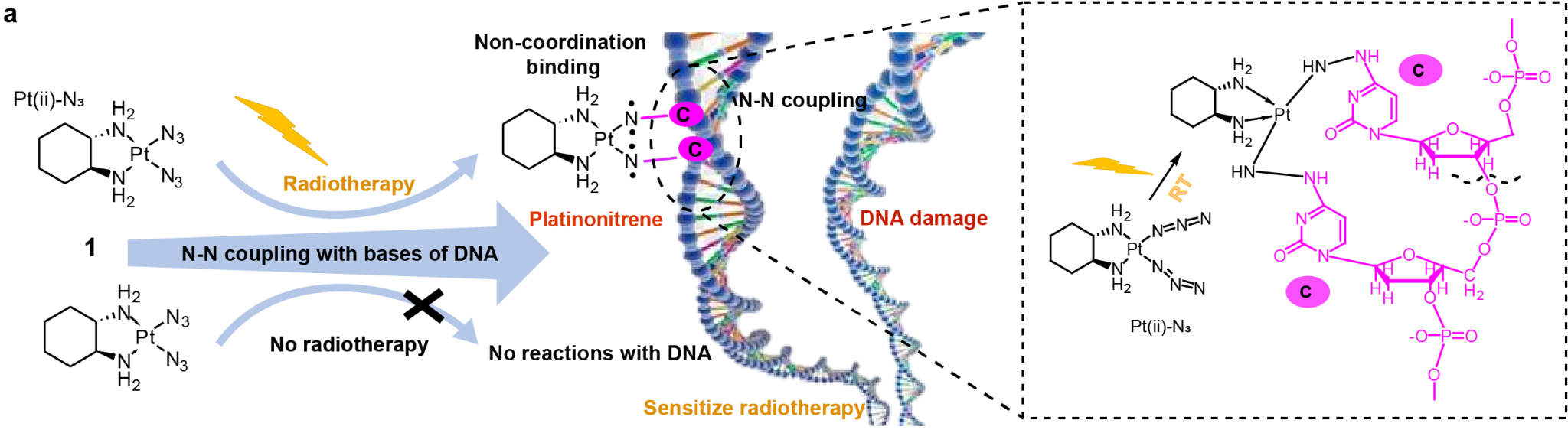
图1. Complex1在放疗下与DNA通过N-N偶联共价结合
针对上述难题,中国科大闵元增教授团队设计合成了一种新型铂系叠氮基配合物,创新性地利用放射线诱导其在肿瘤原位生成高活性铂氮宾中间体(图1),实现了肿瘤部位的精准、可控增敏。该复合物本身无明显毒性,仅在放疗的作用下才会生成铂氮宾并与DNA碱基发生N-N偶联,形成稳定的Pt-N-N-DNA结构,显著增强放射线对肿瘤细胞DNA的损伤效应,且其增敏机制不依赖活性氧。
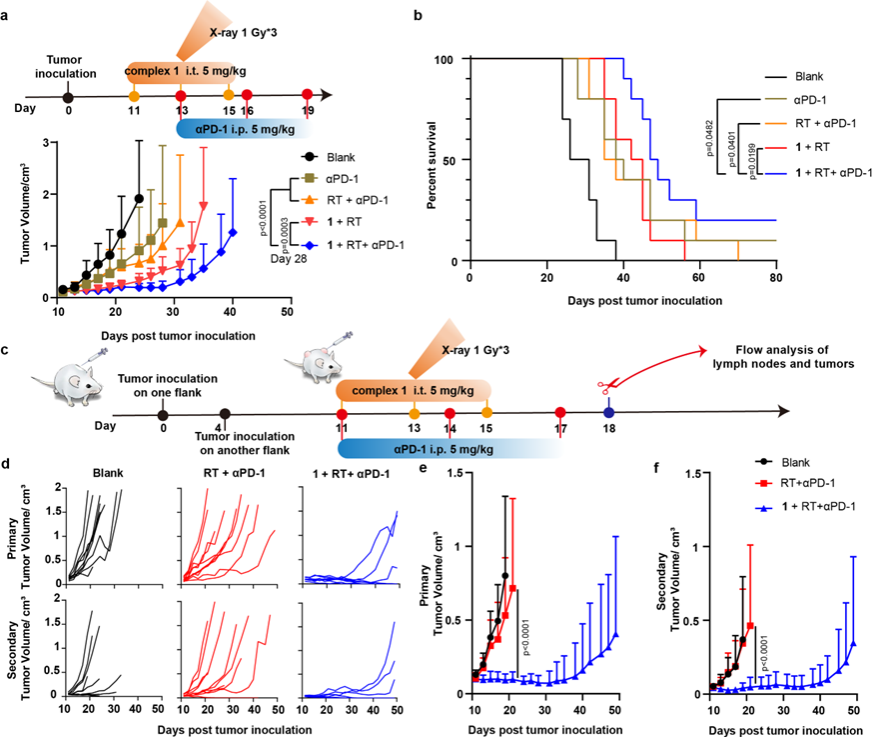
图2. Complex1增敏放疗改善αPD-1治疗与远隔效应
该研究的提出了“放射线诱导原位生成高活性中间体”的放射增敏新范式。这种局部激活策略可最大限度降低全身毒性,同时充分发挥增敏效能,不仅为铂类药物的设计提供了全新方向,也为精准放疗与免疫治疗的协同增效提供了新的技术方案,对推动肿瘤治疗向更安全、更高效、更精准的方向发展具有重要意义。
来源:安徽视讯(2026-03-16) 记者:王丽丽
原文链接:https://console.ahsx.ahtv.cn/web/cms/rmt0087_html/1/clpd/cssh/cszx/260471.shtml?share=true&type=1&articleid=260471