中国科大刘海燕教授、陈泉教授课题组与复旦大学王文宁教授合作,采用蛋白质结构预测、序列设计等计算手段与蛋白质互补分析和深度突变扫描、X射线晶体学、NMR等实验结合的方法,揭示了固有无序的4.1G蛋白C端结构域识别其固有无序靶标的结构机制。相关研究成果以“Combined prediction and design reveal the target recognition mechanism of an intrinsically disordered protein interaction domain”为题,于2023年9月18日发表在《美国科学院院刊》(PNAS)上。
固有无序蛋白(Intrinsically Disordered Protein,IDP)之间的相互作用具有高度动态性。如何阐明其底层的三维结构机制对目前的研究方法是一种挑战。4.1G蛋白作为细胞膜骨架适配器,其保守但被认为是固有无序的C端结构域可以靶向识别其他蛋白中的特定无序区域,在细胞骨架维护、蛋白定位、信号传导、细胞黏附和迁移等过程中发挥重要作用。之前研究发现4.1G蛋白C端结构域与NuMA蛋白C端区域之间存在相互作用,但缺乏明确的结构机制,难以确定该C端结构域所识别的氨基酸序列特性。
在该研究成果中,作者先用基于二氢叶酸还原酶的蛋白质互补分析体系来高效检测无序片段间的相互作用,系统研究了位点突变和截短对互作的影响,发现实验结果与AlphaFold2预测的α/β型复合物结构模型吻合;作者进一步用蛋白质序列设计深度学习模型ABACUS-R基于结构设计了多个突变体,成功获得一个突变体的晶体并解析了其结构。晶体结构与预测模型高度一致,证明两段无序区发生协同折叠,形成包含三段反平行β的折叠片层与一段α螺旋堆积的有序核心结构,其中β折叠片层由来自4.1G的两段无序区包夹来自NuMA的无序靶标片段共折叠形成;进一步分析表明,4.1GC端结构域与其他靶标蛋白的结合采用了类似结构机制(图1)。
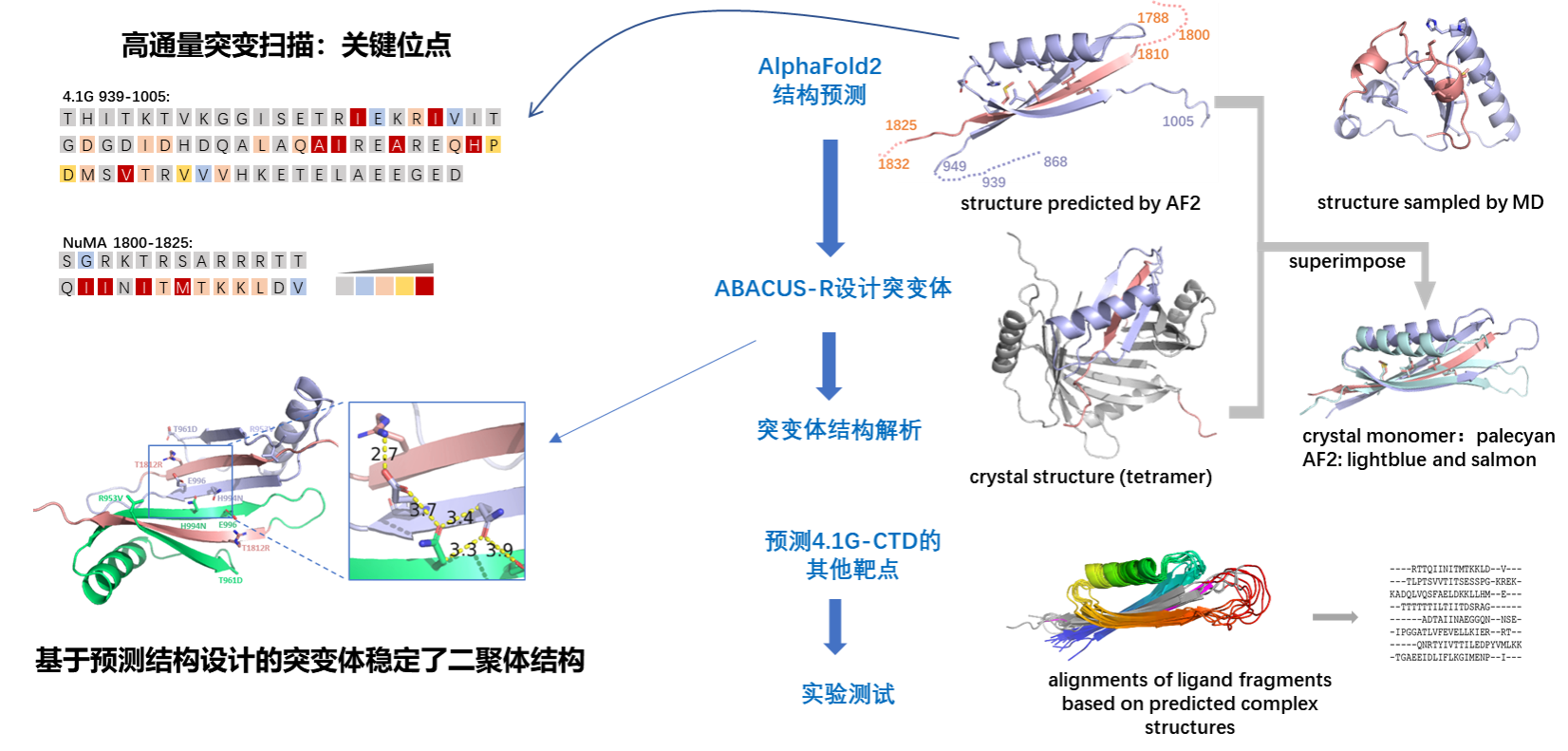
图1.研究流程概述
该研究揭示固有无序蛋白结构域可以用与靶标协同折叠形成α/β型结构的机制来识别多样但具有特定序列特征的无序靶标。该工作采用的计算-实验结合研究策略为解析其它固有无序蛋白互作机制提供了新思路。中国科学技术大学生医部胡秀红博士为本文的第一作者。中国科大生医部刘海燕教授、陈泉教授、复旦大学王文宁教授为本文的共同通讯作者。该研究得到了科技部国家重点研发计划项目、国家自然科学基金项目和中国科学院青年团队计划项目的支持。
原文链接:www.pnas.org/doi/10.1073/pnas.2305603120
(生命科学与医学部)