一氧化氮 (NO)、一氧化碳(CO)和硫化氢(H2S)是生物体内源性气体递质(Gasotransmitter),具有重要的生理/病理功能,同时也具有优异的抗炎和抗菌活性。鉴于气体递质在治疗心脑血管疾病(人类死亡的“头号杀手”)和呼吸系统疾病(如当前全球爆发的新冠肺炎)方面的独特优势和明确疗效,发展气体递质药物受到了广泛关注。不同于传统的固体和液体药物,气体递质不能通过口服、注射、透皮等方式给药;在生理条件下易代谢、半衰期极短,吸入给药后主要作用于肺部,难以到达其它病灶部位。针对上述问题,中国科学技术大学化学与材料科学学院胡进明课题组在气体递质的可控递送方面开展了系列工作,初步探索了气体递质高分子材料在治疗炎症和感染类疾病方面的潜在应用。
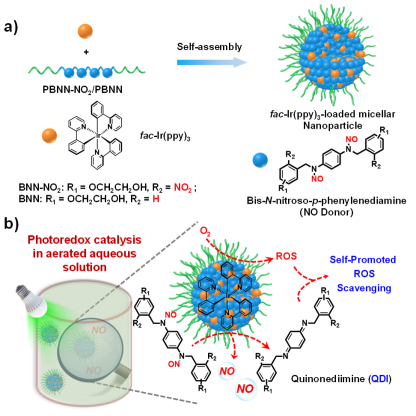
图1、构建耐氧性光氧化还原催化驱动的一氧化氮递送体系。
近期,胡进明课题组与刘世勇教授课题组、肖石燕课题组开展合作,报道了一种耐氧型光氧化还原催化调控NO释放的策略,并成功用于细菌感染治疗。以紫外光吸收N,N′-二亚硝基-1,4-苯二胺类光响应NO释放分子(BNN-NO2和BNN)作为研究对象;研究表明,BNN-NO2和BNN在可见光(500 nm)辐照下被光催化剂三(2-苯基吡啶)合铱(fac-Ir(ppy)3)激活并释放NO。有趣的是,NO释放后BNN-NO2和BNN可自发转化为相应的醌二亚胺(QDI)结构,原位清除产生的活性氧(ROS),实现了独特的氧气耐受性能。虽然光氧化还原催化已广泛用于有机合成中,但在生理环境下利用光氧化还原催化反应激活生物活性分子仍然面临巨大挑战——由于生理环境的复杂性,光氧化还原催化反应往往受到周围生物分子的影响 (如氧气会严重淬灭光催化剂的激发态)。
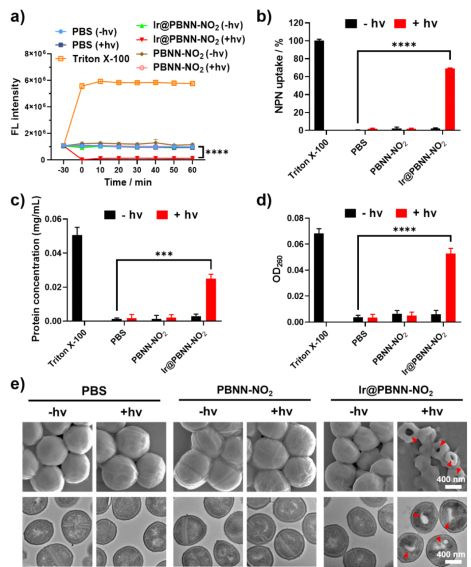
图2、光氧化还原催化触发一氧化氮释放实现细胞膜超极化和菌膜渗透性增强,有效杀灭耐甲氧西林金黄色葡萄球菌(MRSA)。
研究人员通过共聚将BNN-NO2或BNN引入两亲性嵌段聚合物中,负载光催化剂fac-Ir(ppy)3后可得到均匀胶束纳米粒子。在可见光辐照下,在无需额外添加氧气清除剂的条件下成功实现了NO的触发释放,同时伴随着水中溶解氧含量的自发下降。体外抗菌实验结果表明:该NO释放胶束可使细菌膜电位超极化,并增加细菌膜渗透性从而达到杀灭细菌的效果。在小鼠全皮层细菌感染创伤模型中,光氧化还原催化触发NO释放可有效治疗耐甲氧西林金黄色葡萄球菌(MRSA)伤口感染并促进伤口愈合。
本工作为探索光氧化还原催化的生物医学应用提供了有益参考,其独特的氧气耐受性有效避免了生理环境下氧对光氧化还原催化的不利影响。
上述研究工作得到了国家自然科学基金委、科技部重点研发计划和中国科学技术大学培育基金等资助。
相关论文链接:
https://onlinelibrary.wiley.com/doi/10.1002/anie.202204526 (Hot Paper)
https://onlinelibrary.wiley.com/doi/10.1002/anie.202112782(Hot Paper)
https://onlinelibrary.wiley.com/doi/full/10.1002/anie.202107155
https://onlinelibrary.wiley.com/doi/full/10.1002/anie.202104024 (Hot Paper)
https://onlinelibrary.wiley.com/doi/full/10.1002/anie.202010009 (VIP)
(化学与材料科学学院、科研部)